
Hlavně nebýt nudný patron, říká fyzikální chemik
05. 10. 2020
Rád se na téměř zapomenuté a hlavně nedořešené vědecké problémy dívá novýma očima. A vyplácí se mu to. Naposledy Pavel Jungwirth z Ústavu organické chemie a biochemie AV ČR oprášil prastaré pokusy s házením sodíku do vody a kapalného amoniaku. A podařilo se mu detailně popsat přerod nekovu v kov. Rozhovor s fyzikálním chemikem, pro kterého je vedle vlastního bádání důležitá i popularizace vědy, vyšel v novém čísle časopisu Akademie věd ČR A / Věda a výzkum.
Váš nedávný objev se dostal až na titulní stranu prestižního časopisu Science. To je sen každého vědce, nebo ne?
Kdybych to dotáhl na obálku Playboye, bylo by to ještě lepší (směje se). Teď ale vážně: měli jsme s týmem samozřejmě velkou radost, slavili jsme, ale člověk by to neměl moc prožívat. Mým cílem není okupovat titulky magazínů, ale dělat pěknou vědu. Mimochodem, je legrační, že jsme takový úspěch sklidili zrovna s něčím, co začalo spíše jako klukovské hraní či terapie proti pracovnímu vyhoření.

Objev Pavla Jungwirtha se dostal na obálku prestižního časopisu Science.
Co si pod tím představit?
Možná si ze školních hodin chemie pamatujete efektní pokus, kdy učitel obřadně vhodil kousek sodíku do misky s vodou a…
A směs vybouchla!
Přesně tak. Zhruba před osmi lety jsme se s mým britským kolegou Philem Masonem začali ve volném čase tímto klasickým experimentem bavit. Ve škole jsem ho nějak vynechal, takže jsem si tímto způsobem vlastně trochu doháněl pubertu.
Poněkud explozivní zábava. Okolí z vás asi mělo radost.
Měli jsme tehdy naštěstí v práci balkon, který byl na výbušné pokusy ideální. Když jsme se pak přestěhovali do budovy, kde žádný nebyl, podařilo se mi dokonce „vydyndat“ z ředitele ústavu malou laboratoř jen na tyto víkendové kratochvíle. Pak už nás ale přestalo bavit pořád po explozích uklízet. A tak jsme se před pěti lety rozhodli, že zkusíme méně výbušnou cestu a vodu nahradíme tekutým amoniakem.
To ale také nebyla žádná novinka, že?
Vůbec ne, podobné pokusy prováděl anglický chemik sir Humphry Davy už před více než dvěma sty lety. Již tehdy pozoroval, jak sodík v parách amoniaku krásně zmodrá a směs se změní v elektrolyt. Už dlouho se také ví, že když se do kapalného amoniaku alkalického kovu přidá víc, roztok získá zlatavou nebo bronzovou barvu a začne se chovat jako kov. Dosud ale nikdo netuší, co přesně se při té změně děje na molekulové úrovni. Dlouhá léta to bylo velké téma. Po druhé světové válce se dokonce věřilo, že by tak šly připravovat vysokoteplotní supravodiče, což se ale brzy ukázalo jako slepá ulička. Postupně se pak problém úplně vyčerpal, došly techniky, jak ho zkoumat.
Vy jste tedy v podstatě vykopali vědeckou mrtvolu…
Přesně tak. A vyhrabat zombie se vyplatilo! Stačilo se podívat na starou věc současnýma očima a díky tomu se nám podařilo rozkrýt, jak přesně přechod nekovu v kov probíhá. Nekovový systém je spletí izolovaných elektronů, které mohou i za jeho modrou barvu. Oproti tomu kov se skládá z delokalizovaných elektronů, které jsou vzájemně propojené. Je to takový rosol, jenž se dokáže kolektivně hýbat a oscilovat na charakteristické frekvenci, což způsobuje typický kovový lesk a barvu. Nás zajímalo, jak se z izolovaných – chemických – elektronů stanou delokalizované – fyzikální, kovové.
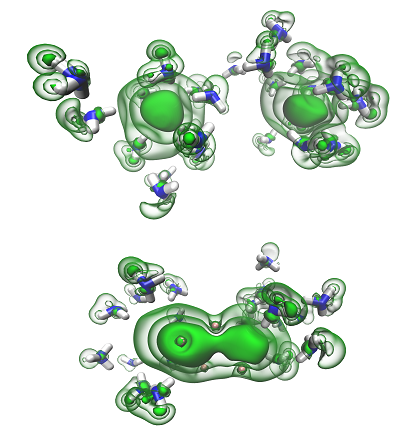
Izolované elektrony v nekovovém roztoku amoniaku se sodíkem (nahoře) se po přidání velkého množství sodíku vzájemně propojují a mění se v elektrony kovové (dole).
Co jste zjistili?
Izolované elektrony si můžete představit jako rozplizlé tenisové míčky. Když přidáte sodíku do amoniaku víc, míčků přibude, začnou se dotýkat a propojovat. Tím vznikne vodivostní pás a roztok získá vlastnosti kovového drátu. Stejně dobře pak vede elektřinu. Zajímavé je, že přechod je pozvolný – není tam žádná přesná hrana, jako když například při konkrétní teplotě taje led na vodu.
Nic z toho se dosud nevědělo?
Ne v detailu, nebylo totiž jak probádat elektronovou strukturu té změny. My jsme to zkusili pomocí fotoelektronové spektroskopie. Ta spočívá v tom, že na látku posvítíte rentgenovým paprskem o definované vlnové délce, vyrazíte z ní elektrony a ty doletí k detektoru, který změří jejich kinetickou energii. Tak zjistíte, jak silně jsou v materiálu jednotlivé elektrony vázané. Funguje to ale jenom ve vakuu a umístit do něj těkavou tekutinu, jakou je právě kapalný amoniak, se dosud považovalo za nemožné. Všechno se ale dá obejít.
Povídejte.
Rozhodli jsme se, že zkusíme amoniak vstřikovat do vakua pomocí mikrotrysek tenčích než lidský vlas. Věřili jsme totiž, že když se tam materiálu dostane jen minimální množství, vakuum se zkazí jen málo a budeme to schopni změřit. Na samotný experiment jsme se v Praze připravovali rok. Až pak jsme vyrazili, abychom si jej zkusili naostro, na berlínský synchrotron BESSY II, kde jsme dostali pět měřicích dní. Jde o neskutečně drahé zařízení velikosti fotbalového stadionu, kde panují striktní bezpečnostní pravidla. Když jsme tam tedy dorazili s kilem sodíku a bombou amoniaku, nebyli z nás němečtí kolegové moc nadšení.
Báli se, že jim to tam vyhodíte do povětří?
Ze začátku ano. Mysleli si, že jsme blázni. Pak se ale pro náš projekt nadchli a začali nám důvěřovat. Makali jsme čtyřiadvacet hodin denně a nakonec to vyšlo – díky metodě mikronástřiků jsme dokázali proměřit elektronovou strukturu celé proměny nekovu v kov. A ještě jsme u toho vyrobili spoustu zmrzliny. Bohužel jen té amoniakové.

Část vakuové aparatury k pokusům s kapalným amoniakem a alkalickými kovy
To asi nebude jedlá lahůdka.
Kdepak. Tato smradlavá žíravá hmota rozhodně není k snědku. Jejímu vzniku jsme se ale nemohli vyhnout. Amoniak je totiž při pokojové teplotě plyn, a když jsme jej chtěli zkapalnit, museli jsme ho zchladit alespoň na minus třicet tři stupňů Celsia. Mikrotrysky jsme proto chladili tekutým dusíkem ve směsi s etanolem. Když z nich pak kapalný amoniak dopadal na chladný povrch, hned zamrzal a z každého experimentu nám tak vzniklo asi půl kila nechutné zmrzky.
Takže o tom, jak se mění nekov v kov, už má lidstvo díky vám jasno.
Ne tak docela. Chybí ještě detailně prozkoumat molekulární strukturu amoniaku při té změně. K tomu je ale třeba provést jiný složitý experiment – neutronový rozptyl. Brzy nás snad čeká další výlet, tentokrát na jaderný reaktor do Grenoblu ve Francii.
K čemu tak důkladné objasnění této reakce poslouží?
Jde o krásný model, na němž se dá ve školách vyučovat přechod mezi chemií a fyzikou. Studenty by mohl nadchnout pro vědu. Pro nás však byla práce s tekutým amoniakem hlavně tréninkem na náš nejvýbušnější sen: přípravu kovové vody.
Vrátíte se tedy zpět k explozím?
Už se nám je podařilo obejít. Zlatý grál tak máme v podstatě na dosah. Problém je, že kovová voda strašně rychle chemicky reaguje. Zatímco kovový amoniak vydrží i den, tato tekutina existuje jen asi dvě vteřiny. A rozhodně jí nevyrobíte kýbl, ale jen tenkou vrstvu na povrchu kapky alkalického kovu. Logicky vás teď asi napadne, k čemu je tedy kovová voda dobrá. Upřímná odpověď zní, že naprosto k ničemu.

Přidáním většího množství sodíku do kapalného amoniaku se roztok zbarví do bronzova.
Proč se s ní pak vůbec trápíte?
Protože vytvořit něco takového je až nemravně krásné. Vnímám vědu tak trochu jako sportovní utkání. K čemu je dobré, že se fotbalista prodere třemi obránci a pak kopne balon do branky? K ničemu, ale když je to pěkné, přijde se podívat spousta lidí. Samozřejmě, že je skvělé vyvinout praktické věci jako vakcínu proti koronaviru, ale udělat něco „jen“ hezkého má podle mě také smysl. Ukážeme tak lidem, že věda umí být krásná, že je součástí širší kultury a že může být zábavná stejně jako třeba sport. A pak zase vymyslíme něco užitečného.
Například jak dostat léky do buněk za pomoci peptidů?
Třeba. Tento náš výzkum má praktický potenciál. Naše peptidy jsou kladně nabité krátké sekvence aminokyselin, které dokážou proniknout do buňky. Dala by se na ně tedy navěsit některá léčiva. Dnes se látky do buňky dostávají pomocí transportního váčku a buňka pak musí vynaložit energii, aby ten pomyslný vagon s nákladem naložila a poté i vyložila. Peptidy se přitom do buněk umí dostat i pasivně. A tento mechanismus se snažíme pochopit a ochočit si ho.
Co by se změnilo, kdyby se to podařilo?
Transport léčiv do buněk by byl efektivnější. Jejich dávka, kterou by pacient musel spolykat, by se tak třeba desetkrát snížila. A s ní i vedlejší účinky. Ale to je ještě opravdu daleko – zatím jsme s mými kolegy v Česku, Německu a Izraeli navěsili na peptid jen fluorescenční barvičku, abychom si posvítili na to, jak vláček projíždí tunelem, tedy jak peptid prochází přes buněčnou membránu. Než případně dojde na léky, čekají nás ještě léta práce s počítačovými simulacemi a elektronovými a fluorescenčními mikroskopy.
Zkoumal jste moře v Kalifornii, bouřkové mraky, fungování mořské vody v atmosféře i ionty solí v lidském těle. Nejste tak trochu vědecký fluktuant?
Ve střídání témat jsem skutečně extrém. Sám sebe proto označuju za vědního turistu, který zvolna přechází od fyziky přes chemii k biologii. Moje výzkumy ale nejsou každý pes jiná ves, jak by se mohlo na první pohled zdát. Spojuje je jeden leitmotiv, a sice nabité částice ve vodě. To je něco, čemu vážně rozumím. Slaná voda je pak vyloženě moje srdeční záležitost.
Prý nezkazíte žádnou zábavu. Je to pravda?
Jsem takový věčný showman. Legrace je podle mě důležitá i při popularizaci vědy, které se hodně věnuju. Osvědčila se mi metoda dvorního šaška. Snažím se říkat vážné věci nevážně, zabalit je do žertu, což je užitečný trik, který dává protistraně možnost informace strávit. Tímto způsobem se dá krásně podtrhnout absurdita špatného postoje a podobně. Chce to ale dovednosti a trénink.

Pavel Jungwirth s rodinou v Karolinu u příležitosti přebírání profesury
Jak se takové šaškování trénuje?
Nacvičuju si třeba dramatičnost projevu, snažím se být ekonomický v mluvení… Zbytečně se nerozkecávat jsem se naučil hlavně díky dlouholetému psaní popularizačních sloupků do Respektu. I dvorní šašek zkrátka musí něco umět, jinak by byl prostě jenom trapný. Základem je ale nebýt nudný patron.
Proto jste si na přebírání profesury do Karolina vzal snowboard, batůžek a PET lahev?
To je veselá příhoda (směje se). Diplom mi předával tehdejší prezident Václav Klaus a já s tím měl z mnoha důvodů morální problém. Tak jsem se ověsil věcmi, které Václav Klaus považoval za znaky levicových intelektuálů, a do kapsy saka jsem si dal obří zvýrazňovač s rokem konce jeho mandátu a smajlíkem. Byla to narážka na tehdy čerstvou kauzu, kdy náš prezident v Chile ukradl protokolární pero. Musím říct, že on se moc nesmál, ale rodinu jsem pobavil královsky.
Máte stále pusu od ucha k uchu, jste vyhlášený optimista. Nenaštval byste se prý, ani kdyby vám někdo ukradl výzkum – bral byste to jako pochvalu. Kam na tak pozitivní přístup chodíte?
Část mého optimismu zřejmě plyne z určité povrchnosti a z toho, že si věci nepřipouštím. Podvědomě samozřejmě chápu, že doba není úplně veselá, ale dokážu to celkem dobře vytěsnit. Mně to vyhovuje, okolí už mnohdy méně. Manželka Ivka mi třeba říká, že se se mnou někdy nedá vydržet. Možná by chtěla, abych byl alespoň občas seriózní vědec. Chápu, že by se to často hodilo víc, než se jenom pořád „tlemit“. Jenže já byl vážný celé dospívání a teď si to prostě vynahrazuju (směje se).
prof. Mgr. PAVEL JUNGWIRTH, CSc., DSc.
Ústav organické chemie a biochemie AV ČR
Působí jako vedoucí skupiny molekulového modelování Ústavu organické chemie a biochemie AV ČR. Zároveň vyučuje na katedře chemické fyziky a optiky MFF UK a předsedá Učené společnosti ČR. Dlouhodobě pracoval na univerzitách v USA, Izraeli, Švýcarsku nebo Finsku. Získal již dvanáct významných tuzemských i zahraničních vědeckých ocenění. Je editorem amerického časopisu Journal of Physical Chemistry a nadšeným popularizátorem vědy. Zabývá se zejména modelováním interakcí iontů s biomolekulami v roztocích.
Celý článek i další zajímavosti si můžete přečíst v časopise A / Věda a výzkum.

3/2020 (verze k listování)
3/2020 (verze ke stažení)
Připravila: Radka Římanová, Divize vnějších vztahů SSČ AV ČR
Foto: Jana Plavec, Divize vnějších vztahů SSČ AV ČR; archiv Ústavu organické chemie a biochemie AV ČR; archiv Pavla Jungwirtha
Přečtěte si také
- S Tomášem Etrychem o polymerech, které umí chirurgům zobrazit zhoubný nádor
- V nanosvětě je zlato modré i rudé, říká Vladimíra Petráková
- Tajemství termitů: dlouhověkost a po miliony let fungující řád
- Plasty by se mohly vyrábět z oxidu uhličitého získaného z atmosféry, říká chemik
- Čeští vědci spolupracují na vývoji ekologických a levných solárních článků
- Nebezpečné látky obsažené v náplních elektronických cigaret poškozují plíce
- Nový vodíkový elektrolyzér ukládá energii z obnovitelných zdrojů
- Chemičkou jsem se chtěla stát už od čtrnácti let, říká Adéla Šimková
- Vědci vyvinuli novou kontrastní látku, která pomůže včas odhalit skryté nemoci
- Rostliny v sobě mají neuvěřitelné chemické bohatství, říká Tomáš Pluskal