Jak překonat rezistenci nádorových buněk na terapii: vědci testovali nový systém
23. 07. 2025
Běžně používané protinádorové léčivo, které se dostane přesně do místa nádoru a úspěšně zdolá způsob, jímž se rakovinné buňky terapii brání. To je podstata nového systému, který ve studii publikované v časopise Journal of Controlled Release představil tým Mikrobiologického ústavu AV ČR a Ústavu makromolekulární chemie AV ČR ve spolupráci s lékaři z Fakultní nemocnice v Motole. Vědci a vědkyně koncept úspěšně otestovali na buňkách i zvířecích modelech. Má proto potenciál stát se součástí moderní onkologické léčby.
Chemoterapie je spolu s chirurgickým zákrokem, radioterapií a imunoterapií jedním ze základních způsobů léčby rakoviny. Velkým problémem je však tzv. mnohočetná léková rezistence. Jedním z jejích častých mechanismů je „pumpování“ léčiva z buňky dřív, než začne působit, pomocí zvláštních transportních proteinů. V membráně řady typů zdravých buněk se vyskytují běžně a umožňují přenos celé řady látek přes membránu buňky. U rezistentních rakovinných buněk se ale některé transportní proteiny v extrémním počtu zmnoží a působení léčiva uvnitř buněk zabrání, protože jsou schopné léčivo úplně nebo téměř úplně z buňky vyloučit.
„Zaměřili jsme se na rezistentní rakovinné buňky, které mají hodně tzv. P-glykoproteinů,“ říká Milada Šírová z Laboratoře nádorové imunologie Mikrobiologického ústavu AV ČR. Nové látky její tým testoval in vitro (ve zkumavce) a také in vivo – na myších. „Díky kolegům z Fakultní nemocnice Motol jsme navíc mohli použít speciální myší model s nádorem klinického původu. Vzorky odebrané z nádorů pacientů totiž mohou za určitých okolností růst v experimentálních myších a lze na nich otestovat účinek léčiva. Možnost takto pracovat se vzorky nádorů pacientů přináší další kvalitu při testování: tento systém je o něco blíže skutečným podmínkám při léčbě. To je velmi důležité pro zhodnocení potenciálu nové látky pro klinické využití,“ zdůrazňuje Milada Šírová.
Cílený systém dopravy léčiv v těle
Zásadním přínosem byla spolupráce biologů – imunologů s chemiky, kteří navrhli, připravili a charakterizovali dopravní systém pro léčivo na bázi syntetických kopolymerů. Tyto speciální amfifilní kopolymery (PHPMA-b-PPO) se ve vodném prostředí samy skládají do micel – malých kulovitých struktur schopných pasivně zacílit léčivo přímo do oblasti nádorové tkáně. „Do těchto struktur jsme navázali doxorubicin – běžné cytostatikum používané k léčbě rakoviny. Kopolymer jej dokáže přesně nasměrovat do nádoru. To je klíčové pro to, aby byl lék účinný a vedlejší účinky léčby co nejméně zatížily zdravé tkáně pacienta,“ vysvětluje Tomáš Etrych, vedoucí Oddělení biolékařských polymerů Ústavu makromolekulární chemie AV ČR.
Omezení zdroje energie v rakovinné buňce
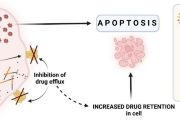
K vylučování nežádoucích látek z buněk (toxiny, metabolity, léčiva) využívají buňky energii ve formě ATP. ATP je klíčová molekula potřebná pro fungování většiny buněčných procesů. Jejím zdrojem jsou mitochondrie, jež zajišťují kromě tvorby ATP i buněčné dýchání. Testy prokázaly, že připravené polymerní systémy ovlivnily funkci mitochondrií, způsobily snížení hladiny ATP v rakovinné buňce a tím omezily její schopnost bránit se protinádorové léčbě.
Studii publikovanou v časopise Journal of Controlled Release podpořil projekt Ministerstva zdravotnictví ČR a Národní ústav pro výzkum rakoviny.
Odkaz na publikaci:
https://www.sciencedirect.com/science/article/pii/S0168365925002652?via%3Dihub#f0040, Volume 381, 10 May 2025, 113645
Více informací:
RNDr. Milada Šírová, Ph.D.
Mikrobiologický ústav AV ČR
sirova@biomed.cas.cz
+420 296 442 364
RNDr. Tomáš Etrych, DSc.
Ústav makromolekulární chemie AV ČR
etrych@imc.cas.cz
prof. MUDr. Jan Bouček, Ph.D.
Klinika ORL a chirurgie hlavy a krku
1. lékařská fakulta Univerzity Karlovy a Fakultní nemocnice v Motole
jan.boucek@fnmotol.cz
Přečtěte si také
- Kočka divoká je zpět: v Lužických horách letos úspěšně vyvedla mláďata
- Konference PLATOSpec uzavřela první rok provozu spektrografu
- Když se smlouvy mohou měnit: dopady flexibilnějších pravidel na veřejné zakázky
- Mechorost jako predátor. Výstava ukazuje krásy vědy i humor
- Motýl je značkou nové biotechnologické firmy Taveren Therapeutics
- Nenápadné borelie: vědci popsali první okamžiky infekce lymské boreliózy
- Světové prvenství české vědy: stárnutí vajíček lze zvrátit
- Mezinárodní soutěž Dream Chemistry Award poprvé v historii vyhrál Čech
- Vědci objasnili, jak rostlinné buňky spouštějí životně důležité procesy
- V Praze začíná mezinárodní konference o rentgenové optice v astronomii
Matematika, fyzika a informatika
Vědecká pracoviště
- Astronomický ústav AV ČR
Fyzikální ústav AV ČR
Matematický ústav AV ČR
Ústav informatiky AV ČR
Ústav jaderné fyziky AV ČR
Ústav teorie informace a automatizace AV ČR
Fyzikální výzkum pokrývá široké spektrum problémů, od základních složek hmoty a fundamentálních přírodních zákonů, zahrnující i zpracování dat z velkých urychlovačů, až po fyziku plazmatu při vysokých tlacích a teplotách, fyziku pevných látek, nelineární optiku a jadernou fyziku nízkých a středních energií. Astrofyzikální výzkum se soustřeďuje na výzkum Slunce – především erupcí, na dynamiku těles slunečního systému a na vznik hvězd a galaxií. V matematice a informatice se studují jak vysoce abstraktní disciplíny jako logika a topologie, tak i statistické metody a diferenciální rovnice a jejich numerická řešení. Přitom i čistě teoretické výzkumy v oblastech, jakou jsou např. neuronové sítě, optimalizace a numerické modelování, bývají často motivovány konkrétními problémy nejen v přírodních vědách. Sekce zahrnuje 6 ústavů s přibližně 1600 zaměstnanci, z nichž je asi 630 vědeckých pracovníků s vysokoškolským vzděláním.