Vývoj nových léků bude rychlejší a levnější. Díky vědcům z Fyzikálního ústavu
17. 05. 2019
Vědci z Fyzikálního ústavu Akademie věd ČR publikovali v prestižním americkém časopise Science. Jejich výzkum, na kterém se podíleli i odborníci z Vysoké školy chemicko-technologické a z farmaceutické společnosti Zentiva, se týká nových možností využití rozptylu elektronů na nanokrystalických materiálech.
Základem nové, vylepšené metody je takzvaná absolutní konfigurace molekul organických sloučenin, tedy i těch, které se využívají jako léčiva. Krystaly těchto molekul byly pro současné metody příliš malé. Výsledky tak mohou přispět k levnějšímu a rychlejšímu vývoji nových léků.
Zájem farmaceutických firem
„Určení absolutní konfigurace nově syntetizovaných molekul, které tvoří krystaly pouze v nanorozměrech, bylo doposud velice obtížné, ovšem pro vývoj léků zcela nezbytné, neboť dozorové orgány jako např. U. S. Food and Drug Administration tuto informaci před schválením léku pro trh vyžadují. Naše práce přichází s novým, obecně použitelným postupem, jak určit absolutní konfiguraci organických molekul,“ říká Petr Brázda, hlavní autor článku.
Výzkumné laboratoře tuto metodu budou moci používat a jejich výzkum se zrychlí, zjednoduší a zefektivní. „Už nyní registrujeme zájem farmaceutických firem o používání naší metody,“ doplňuje Lukáš Palatinus.
Absolutní konfiguraci molekul je nutné určovat u tzv. chirálních molekul. Chirální molekula je taková, jejíž zrcadlový obraz se má k původní molekule jako levá ruka k pravé – jsou si velmi podobné, ale nejsou stejné. Z takovýchto molekul jsou tvořeny všechny sacharidy, bílkoviny nebo DNA v živých organismech. Pokud bychom zaměnili chirální molekulu za její zrcadlový obraz, neplnila by v živém organismu svou funkci.
Tajemství krystalografie
Léčiva jsou v současné době většinou chirální molekuly a mezi účinkem molekul, které jsou si zrcadlovým obrazem, bývá značný rozdíl. Zatímco jedna má terapeutický účinek, druhá ho může mít velice malý, žádný nebo může být dokonce tělu nebezpečná. To je také známý případ léku Contergan, jehož jedna molekula působí proti těhotenské nevolnosti, zatímco druhá způsobuje poškození nenarozeného dítěte.
Na příkladu vhodných a nevhodných léčiv lze vidět, jak zásadní je znalost krystalové struktury pevných látek pro pochopení a vysvětlení jejich vlastností. Strukturní krystalografie, jak se tento obor nazývá, je špičkovou doménou vědců z oddělení strukturní analýzy Fyzikálního ústavu AV ČR. Letošní publikací v v časopise Science autoři navázali na dva roky starý úspěch, kdy se dostali přímo na obálku tohoto časopisu. Tým pod vedením Lukáše Palatinuse tehdy zásadně vylepšil metodu určování poloh atomů v nanokrystalech pomocí rozptylu (difrakce) elektronů, což bylo do té doby velmi obtížné. Nyní čeští vědci rozšířili uplatnění této metody i v oborech, kde je nezbytná znalost absolutní konfigurace organických molekul – např. farmaceutický průmysl nebo molekulárně-biologický výzkum.
Mgr. Petr Brázda, Ph.D. – vystudoval anorganickou chemii na Přírodovědecké fakultě (PřF) UK, doktorský titul získal na PřF UK/Université L. Pasteur ve Štrasburku. Po doktorátu pracoval v Ústavu anorganické chemie AV ČR a od roku 2014 je členem skupiny elektronové krystalografie vedené L. Palatinusem na FZU AV ČR. Jako člen týmu získal Cenu Akademie věd za vynikající vědecké výsledky a jako spoluautor publikace cenu Evropské mikroskopické společnosti „Outstanding Paper Award 2017 Instrumentation and Technique Development“.
Dr. Lukáš Palatinus - vystudoval mineralogii a geochemii na Přírodovědecké fakultě UK, doktorský titul získal na Univerzitě v Bayreuthu a pracoval na EPFL Lausanne ve skupině prof. Gervaise Chapuise. Od svého návratu z Lausanne v roce 2009 již pracuje trvale na FZU v oddělení strukturní analýzy, kde vede skupinu elektronové krystalografie. Za svou činnost je mj. držitelem Ceny Neuron, ceny Evropské mikroskopické společnosti „Outstanding Paper Award 2017 Instrumentation and Technique Development“ a vedl tým, který získal Cenu Akademie věd za vynikající vědecké výsledky.
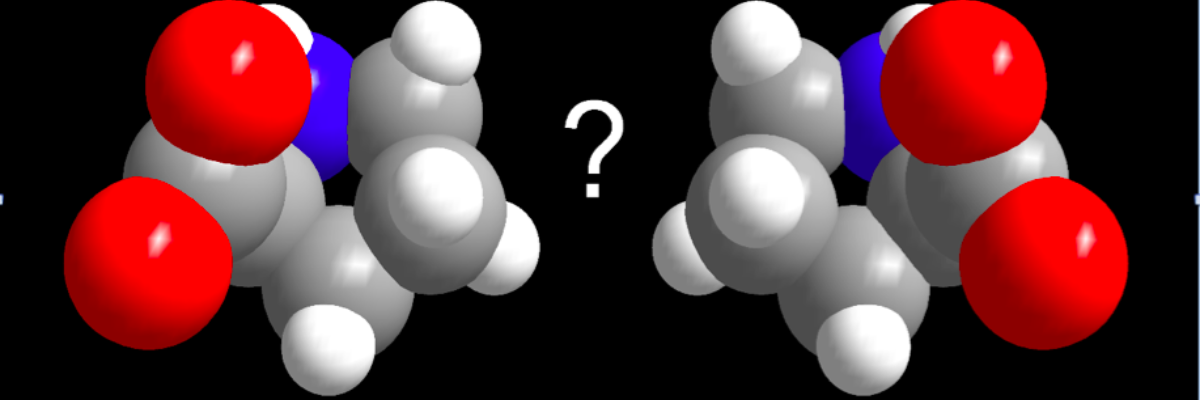
Na titulním obrázku dvě různé absolutní konfigurace molekuly prolinu (označované jako L- a D-prolin) jsou si vzájemně zrcadlovými obrazy (chirální). V živých organizmech se vyskytuje pouze L-prolin. Rozptylem elektronů na nanokrystalech se vědcům podařilo určit, jaká z molekul se v připraveném léčivu nachází.
Připravily: Markéta Růžičková a Alice Horáčková, Odbor mediální komunikace Kanceláře AV ČR ve spolupráci s Mílou Moudrou, Fyzikální ústav AV ČR
Foto: Fyzikální ústav AV ČR
Přečtěte si také
- Věda musí mít podporu, aby přinášela výsledky, zaznělo na Akademickém sněmu
- Hodnocení „šité na míru“: vědecké naděje se seznámily s jeho principy
- Umění spojovat. Tři vědci převzali za svou práci medaile Akademie věd ČR
- Tým z Akademie věd objasnil modrou hádanku a získal Cenu Wernera von Siemense
- Podílel se na přelomovém výzkumu. Nyní archeolog Vitalii Usyk působí v AV ČR
- Program Akademie věd PRAK usnadní cestu jedenácti projektů do praxe
- Liberecký kraj přispěje na výstavbu nové budovy výzkumného centra TOPTEC
- Akademii věd navštívil šachový velmistr a ruský exilový politik Garry Kasparov
- Akademie věd ČR podpoří vědce, kteří nemohou ve své zemi svobodně bádat
- Publikace Nakladatelství Academia zvítězily v soutěži Slovník roku